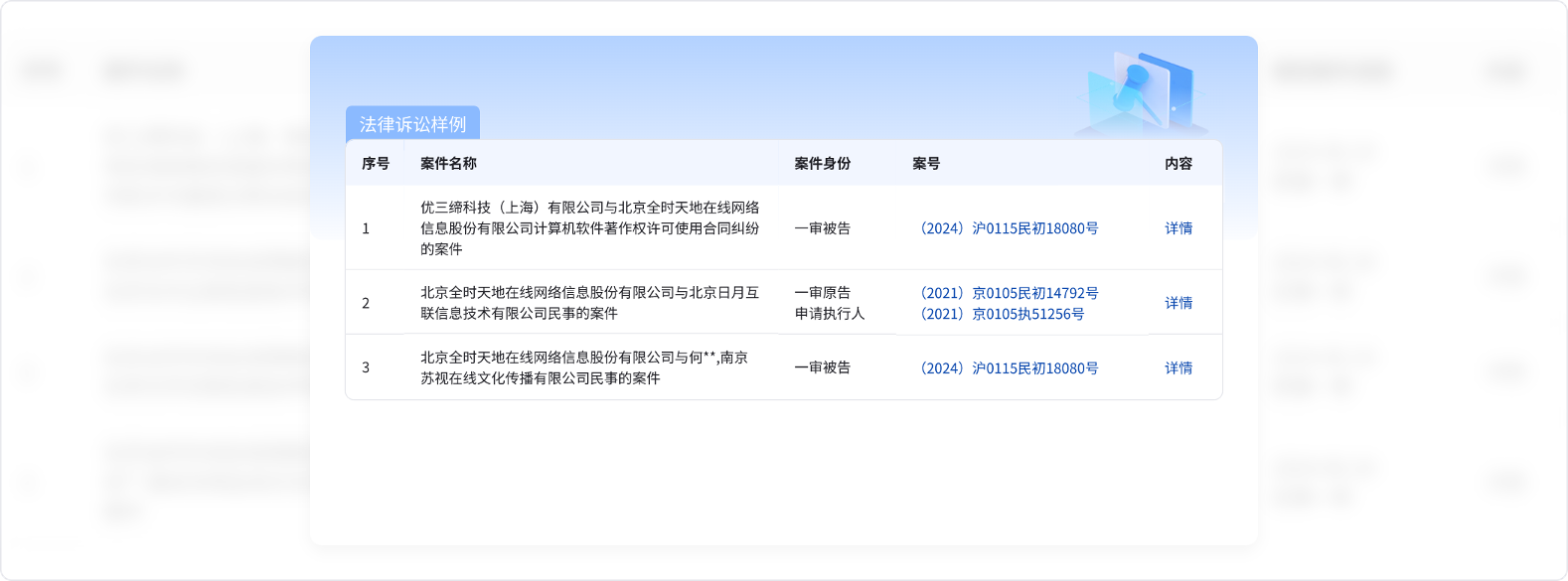
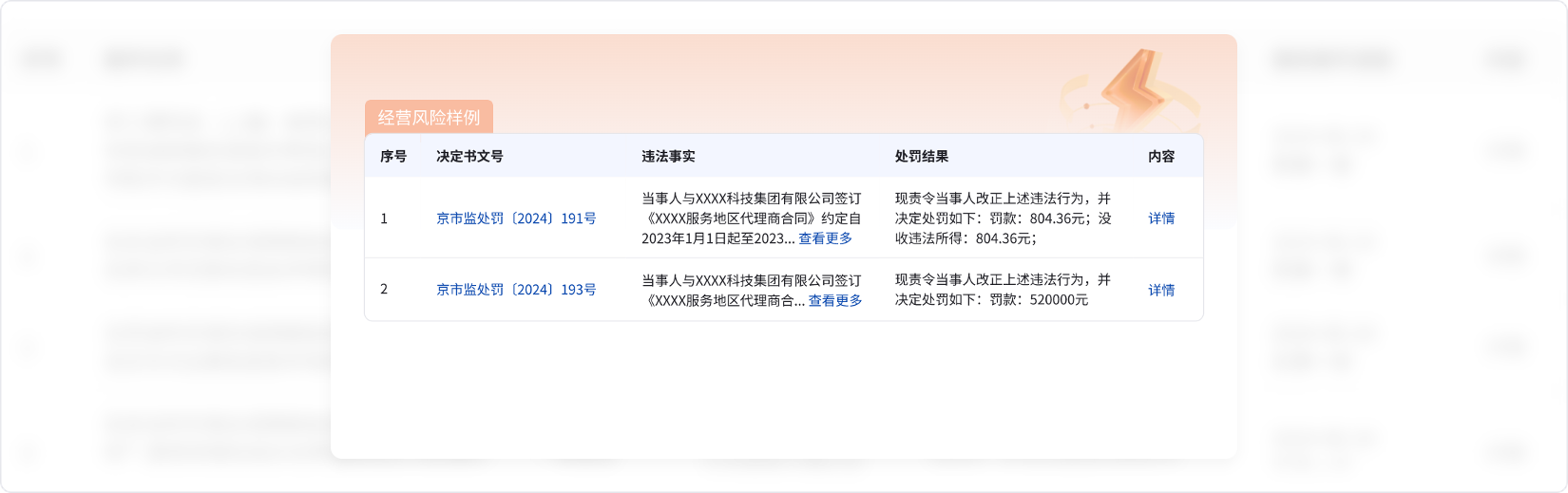
貼上您的名片
掃描二維碼進入虎易小程序投放名片,只需充值少量虎幣,即可張貼名片至
該產品“同類優質商家”欄目下,以相當低的成本獲得大量曝光。
投放說明
>
名片曝光使用說明
步驟1:創建名片
微信掃描名片二維碼,進入虎易名片小程序,使用微信授權登錄并創建您的名片。
步驟2:投放名片
創建名片成功后,將投放名片至該產品“同類優質商家”欄目下,即開啟名片曝光服務,服務費用為:1虎幣/天。(虎幣充值比率:1虎幣=1.00人民幣)
關于曝光服務
名片曝光只限于使用免費模板的企業產品詳細頁下,因此當企業使用收費模板時,曝光服務將自動失效,并停止扣除服務費。
<
返回首頁
稀土火法冶金技術分為三大類:熔鹽電解、金屬熱還原和火法提技術。
稀土火法冶金
(
rare
earths
pyrometallurgy)
技術是指應用高溫這一重要的熱力學條
件,
完成還原稀土離子成金屬態和金屬提的過程。
此過程沒有水溶液參加,
故又稱為火法
冶金。
火法冶金工藝過程簡單,
生產率較高。
稀土火法冶煉主要包括硅熱還原法制取稀
土合金,
熔鹽電解法制取稀土金屬或合金,
金屬熱還原法制取稀土合金等。
火法冶金的共同
特點是在高溫條件下生產。
稀土金屬的制備方法有:①金屬熱還原法。常用鈣、鋰、鈉、鎂等金屬做還原劑,還原
稀土金屬的鹵化物。②熔鹽電解法。可電解稀土鹵化物與堿金屬、堿土金屬鹵化物的熔鹽。
進一步制可采用真空熔煉法、真空蒸餾法、電遷移法和區域熔煉法
。
二:稀土氯化物電解制取稀土金屬
2.1
氯化物熔鹽電解的基本原理
根據電解質能夠發生電離的原理,
由
RECl
:
—
KCl
組成的電解質,
在熔融狀態下也會發
生電離作用,化合物離解為能自由運動的陽離子和陰離子。
氯化稀土將按如下方式離解
RECl
3
=
RE
3
十
十
3C1
—
-
氯化鉀將按如下方式離解:
KCl
=
K
十
十
C1
—
在直流電場的作用下,電解質中的陽離子
K
十
、
RE
3
十
都朝電解槽的陰極運動,而陰離
子
Cl
—則向電解槽的陽極移動,結果在靠近陰極的電解質層中,集中有大量的陽離子,在
靠近陽極的電解層中,
集中有大量的陰離子。
在稀土氯化物電解條件下,
陽離子中的稀土離
子
RE3
獲得電子生成稀土金屬,在陰極上的電化學反應為:
RE
3
十
十
3e
一
=
RE
陰離子中的氯離子
C1
—則在陽極上失去電子,
并生成氯氣
(C12)
,
在陽極上的電化學反
應為:
2C1
—
一
2e
—
===Cl
2
3C1
—
—
3e
—
===3/2 C1
2
這樣,
電解的結果,
在陰極上使得到稀土金屬,在陽極上放出氯氣,
而消耗了氯化稀土和直
流電。電解過程中的總反應式可以表示如下:
RECl
3
===RE 3/2 C1
2
2.2
稀土氯化物電解原料和電解質
稀土氯化物電解原料是把稀土氯化物和氯化鉀按一定比例配制
(
一般氯化稀土重量為
35
—
50
%
)
構成熔鹽電解體系。常用作電解質的主要是堿金屬和堿土金屬的氯化物。
電解用的氯化稀土有三種:結晶料
(RCl
:
·
6H20)
;
脫水料;加碳氯化料。
2.3
電解過程
大致可以分成如下三個階段;
(1)
較稀土金屬平衡電位更正的區間,